Οι αυτοάνοσες ρευματικές παθήσεις (AΡΝ) αποτελούν μια ετερογενή ομάδα διαταραχών που χαρακτηρίζονται από εμπλοκή πολλαπλών οργάνων που προέρχονται από συστηματική φλεγμονή και απορρύθμιση του ανοσοποιητικού συστήματος με επακόλουθη βλάβη των
ιστών.
Τα ΑΡΝ περιλαμβάνουν πάνω από 80 νοσήματα, μεταξύ των οποίων συγκαταλέγονται ο Συστηματικός Ερυθηματώδης Λύκος (ΣΕΛ), η Συστηματική σκληροδερμία (SSc), Ρευματοειδής Αρθρίτιδα (RA), οι φλεγμονώδεις ιδιοπαθείς μυοπάθειες (IIMs) και οι
συστηματικές αγγειίτιδες, η Ψωριασική Αρθρίτιδα κ.ά.
Η επιταχυνόμενη αθηροσκλήρωση και η στεφανιαία μικροαγγειακή δυσλειτουργία (CMD) είναι οι κύριες αιτίες εμπλοκής του καρδιαγγειακού (CV) σε αυτούς τους ασθενείς, οδηγώντας σε αυξημένη καρδιαγγειακή νοσηρότητα και θνησιμότητα.
Στη βιβλιογραφία σχετικά με τις επιπτώσεις του καρδιαγγειακού κινδύνου (CV) στα AΡΝ, δόθηκε αρχικά μεγάλη προσοχή στο ρόλο της φλεγμονής στην πρόκληση επιταχυνόμενης αθηροσκλήρωσης – ιδιαίτερα στον ΣΕΛ και τη ΡΑ – ενώ η εμφάνιση στεφανιαίας
μικροαγγειακής δυσλειτουργίαs (CMD) έχει διερευνηθεί μόνο πιο πρόσφατα.
Στο πλαίσιο των AΡΝ, η στεφανιαία μικροαγγειακή νόσος εμφανίζεται λόγω πολλών μηχανισμών που έχουν περισσότερες ή λιγότερες επιπτώσεις ανάλογα με την υποκείμενη νόσο. Yπάρχει μια άμεση επίδραση της χρόνιας φλεγμονής που οδηγεί σε αγγειοπάθεια μέσω της ενδοθηλιακής βλάβης.
Επιπλέον, υπάρχει μια επίδραση της χρόνιας αυτοάνοσης ενεργοποίησης που μπορεί να οδηγήσει σε μυοκαρδίτιδα, με διάχυτο διάμεσο οίδημα, οδηγώντας τελικά σε μικροαγγειακή ισχαιμία.
Η ενδοθηλιακή δυσλειτουργία πιστεύεται ότι είναι ένα πρώιμο συμβάν στην παθογένεση τόσο της μακρο- όσο και της μικροαγγειακής καρδιακής συμμετοχής στα ΑΡΝ.
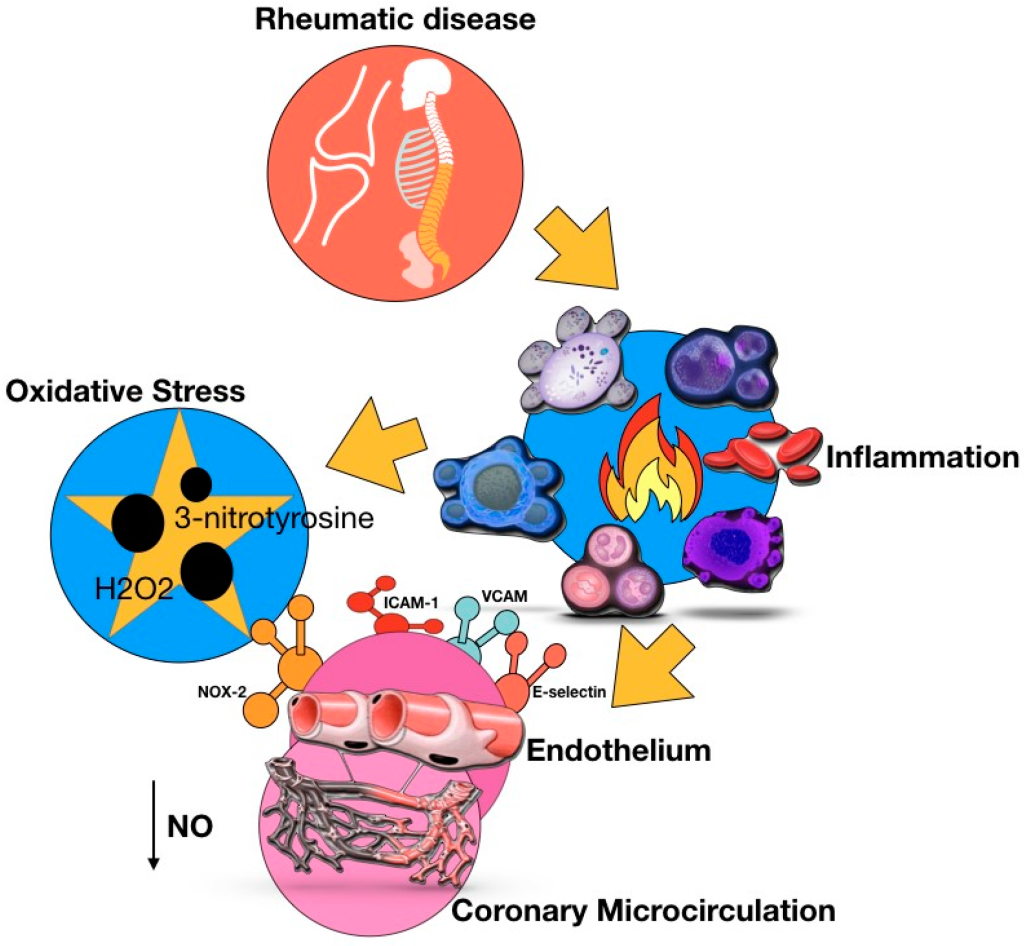
Η μειωμένη βιοδιαθεσιμότητα του μονοξειδίου του αζώτου (NO) και η αυξημένη παραγωγή δραστικών ειδών οξυγόνου (ROS) φαίνεται να είναι ο σύνδεσμος μεταξύ των προφλεγμονωδών μορίων (π.χ. παράγοντας νέκρωσης όγκου-α, ιντερλευκίνες (IL) 1β και 6) με την ενδοθηλιακή δυσλειτουργία σε αυτά ασθενείς (Εικ. 1). Μια απορρύθμιση των μονοκυττάρων (κύτταρα του Ανοσοποιητικού Συστήματος) με παραγωγή IL-1β και η
επέκταση των τοξικών Τ-λεμφοκυττάρων (CD4+ CD28), ένα υποσύνολο CD4+ λεμφοκυττάρων με ισχυρή κυτταροτοξική δράση, είναι επίσης αποδεδειγμένοι μοριακoί μηχανισμοί που εμπλέκονται στην στεφανιαία μικροαγγειακή δυσλειτουργία στα ΑΡΝ (CMD-ARDs).
Εικ. 1
Η στεφανιαία μικροκυκλοφορία περιλαμβάνει προ-αρτηρίδια (διάμετρος 100–500 μm) και αρτηρίδια (διάμετρος < 100 μm) και είναι υψίστης σημασίας για τον προσδιορισμό της αιμάτωσης του μυοκαρδίου, καθώς αντιπροσωπεύει το 80% της συνολικής αντίστασης στη
ροή του αίματος στην καρδιά.
Η στεφανιαία μικροαγγειακή δυσλειτουργία (CMD) αντανακλά την αδυναμία της καρδιακής μικροκυκλοφορίας να διασταλεί κατάλληλα για να καλύψει τη ζήτηση οξυγόνου του μυοκαρδίου λόγω λειτουργικής βλάβης ή δομικής βλάβης της στεφανιαίας μικροκυκλοφορίας.
Σε ασθενείς με Aυτοάνοσα Ρευματικά Νοσήματα με φυσιολογικές στεφανιαίες αρτηρίες, η στεφανιαία μικροαγγειακή δυσλειτουργία (CMD) είναι αρκετά συχνή οκαι υπεύθυνη για αυξημένο κίνδυνο καρδιαγγειακών επεισοδίων και θανάτου, ανεξάρτητα από τους
παραδοσιακούς παράγοντες καρδιαγγειακού κινδύνου.
Η φλεγμονή σχετίζεται με την παθογένεση της συσχέτισης ΑΡΝ με στεφανιαία μικροαγγειακή
δυσλειτουργία (CMD-ARDs), ειδικά σε ασθενείς που έχουν προσβληθεί από ΣΕΛ και ΡΑ, και, ως εκ τούτου, μια πιο επιθετική θεραπευτική προσέγγιση με ανοσοτροποποιητικούς και βιολογικούς παράγοντες μπορεί να αποδειχθεί χρήσιμη σε αυτούς τους ασθενείς για την πρόληψη της διαστολικής και συστολικής δυσλειτουργίας.
ΣΥΜΠΕΡΑΣΜΑΤΙΚΑ
Η στεφανιαία μικροαγγειακή νόσος (CMD )είναι συχνή σε ασθενείς με Α,Ρ.Ν, οδηγώντας σε αυξημένο καρδιαγγειακό κίνδυνο.
Η έγκαιρη αναγνώρισή της και η ακριβέστερη αποσαφήνιση των παθογενετικών μηχανισμών που εμπλέκονται στην στεφανιαία μικροαγγειακή νόσο στα ΑΡΝ (CMD-ARDs) είναι πρωταρχικής σημασίας σε αυτούς τους ασθενείς για τον καθορισμό της βέλτιστης
θεραπευτικής στρατηγικής και την αποφυγή σημαντικών καρδιαγγειακών συμβάντων.
ΒΙΒΛΙΟΓΡΑΦΙΑ
Curr Vasc Pharmacol. 2020
Curr Vasc Pharmacol. 2020
Pharmacol Res. 2022
Curr Vasc Pharmacol. 2020












































